อะตอม หน่วยย่อยพื้นฐานของสรรพสิ่ง ประกอบไปด้วยอนุภาคย่อยอีก 3 ชนิด ได้แก่ โปรตอน นิวตรอน และอิเล็กตรอน แต่ละชนิดมีบทบาทสำคัญต่อคุณสมบัติและพฤติกรรมของอะตอม บทความนี้จะพาน้องๆ ไปทำความรู้จักกับอนุภาคทั้ง 3 ชนิดนี้ครับ
Table of Contents

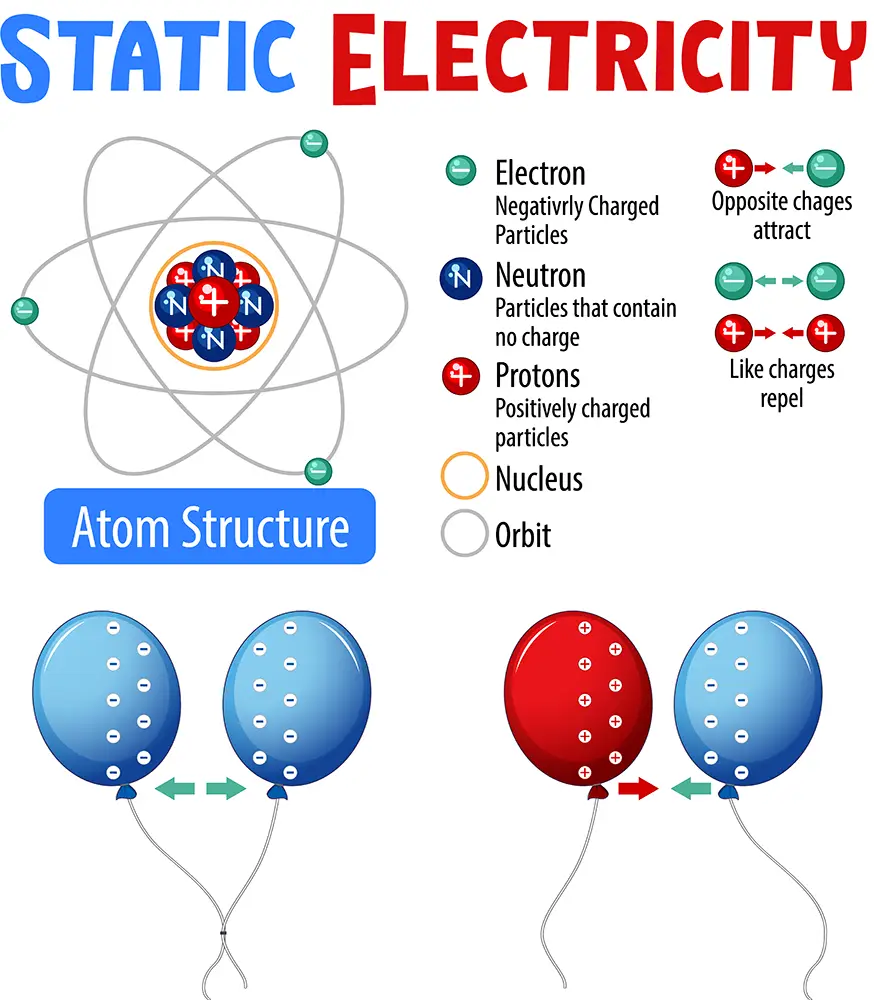
อนุภาคมูลฐานของอะตอม
1. โปรตอน (+)
- อยู่ในนิวเคลียสของอะตอม
- มีประจุไฟฟ้าบวก
- จำนวนโปรตอน (เลขอะตอม) กำหนดชนิดของธาตุ
- มวลประมาณ 1 amu
2. นิวตรอน (n)
- อยู่ในนิวเคลียสของอะตอม
- ไม่มีประจุไฟฟ้า
- มีมวลประมาณ 1 amu
- ร่วมกับโปรตอน กำหนดเลขมวลของอะตอม
- มีผลต่อเสถียรภาพของนิวเคลียส
3. อิเล็กตรอน (-)
- อยู่ในวงโคจรรอบนิวเคลียส
- มีประจุไฟฟ้าลบ
- จำนวนอิเล็กตรอนโดยทั่วไป เท่ากับจำนวนโปรตัน (ยกเว้นไอออน)
- มวลน้อยมาก (ประมาณ 1/1836 ของโปรตอน)
- กำหนดคุณสมบัติทางเคมีของอะตอม
อิเล็กตรอน 1 ตัว หนักกี่กรัม?
อิเล็กตรอน 1 ตัว มีมวลประมาณ 9.109 x 10^-28 กรัม ซึ่งน้อยมาก compared กับมวลของอะตอม
มวลของอะตอมส่วนใหญ่มาจากโปรตอนและนิวตรอน ซึ่งมีมวลมากกว่าอิเล็กตรอนประมาณ 1836 เท่า
ตัวอย่าง
- อะตอมไฮโดรเจน 1 อะตอม มีมวลประมาณ 1.673 x 10^-24 กรัม
- อิเล็กตรอน 1 ตัว มีมวลประมาณ 9.109 x 10^-28 กรัม
ดังนั้น มวลของอิเล็กตรอน คิดเป็นเพียง 0.000544% ของมวลอะตอมไฮโดรเจน 1 อะตอม
| คุณสมบัติ | โปรตอน | นิวตรอน | อิเล็กตรอน |
| ประจุไฟฟ้า | + | 0 | – |
| มวล | ≈ 1 amu | ≈ 1 amu | ≈ 0 amu |
| ตำแหน่ง | นิวเคลียส | นิวเคลียส | โคจรรอบนิวเคลียส |
ความสัมพันธ์ของอนุภาคทั้ง 3
- โปรตอนและนิวตรอนรวมกันเรียกว่า นิวเคลียส
- อิเล็กตรอนโคจรรอบนิวเคลียส
- แรงดึงดูดระหว่างโปรตอนกับอิเล็กตรอน ยึดอะตอมให้คงอยู่
โปรตอน นิวตรอน และอิเล็กตรอน เป็นองค์ประกอบสำคัญของอะตอม แต่ละชนิดมีหน้าที่และบทบาทเฉพาะ ส่งผลต่อคุณสมบัติและพฤติกรรมของอะตอม การเข้าใจโครงสร้างอะตอม ช่วยให้เข้าใจหลักการทางเคมีมากขึ้น
อยากเรียนรู้เพิ่มเติม ติวเคมีสอบเข้า ม.4, เน้นเนื้อหาเคมี ม.ปลาย, เตรียมสอบ TCAS ที่ dekwiz มีคอร์สที่หลากหลายตรงความต้องการแน่นอน!
สมัครคอร์สเรียนเคมีครูกุ๊ก เรียนออนไลน์ พร้อมหนังสือส่งตรงถึงบ้าน
สอบถามเพิ่มเติมได้ที่ Line: @dekwiz