วิชาเคมีของ ม.4 เทอม 1 จะเรียน 6 เรื่องพื้นฐาน (คือ อะตอม ตารางธาตุ พันธะเคมี โมลและสูตรเคมี สารละลาย และปริมาณสารสัมพันธ์) ก่อน เพื่อที่จะไปต่อยอดเนื้อหาของ ม.5-6 ครูจะเล่าภาพรวมคร่าวๆของแต่ละเรื่องให้น้องอ่านจบได้ใน 4-5 นาที
1. อะตอม
อะตอม จะแบ่งเป็น 2 หัวข้อหลัก คือ “อะตอมประกอบขึ้นจากอะไร” กับ “แต่ละธาตุมีอะตอมต่างกันตรงไหน”
อะตอมประกอบขึ้นจากอะไร
ครึ่งแรกจะพูดถึง อะตอมประกอบขึ้นจากอะไร คล้ายๆ วิชาประวัติศาสตร์ เล่าถึงนักวิทยาศาสตร์ในอดีตว่ามีใครทำอะไร ประดิษฐ์สิ่งใด ทดลองแบบไหน ค้นพบอะไร แต่ละคนก็ได้เสนอแนวคิด ทฤษฎี หรือแบบจำลองอะตอม พัฒนาต่อยอดกันมาเรื่อยๆ เริ่มจาก อะตอมกลมๆ ตันๆ ที่ไม่มีอะไรอยู่ข้างใน ไล่มาเรื่อยๆ จนค้นพบว่ามี อนุภาคย่อย (อิเล็กตรอน โปรตอน และนิวตรอน) อยู่ในอะตอม แล้วเจ้าพวกอนุภาคย่อยนี้มันอยู่กันยังไง โดยจะเน้นไปที่อิเล็กตรอนว่ามันมีระบบการจัดเรียงตัวยังไงในอะตอม (การจัดเรียงอิเล็กตรอน) ซึ่งจะเกี่ยวโยงกับเนื้อหาในครึ่งหลัง
แต่ละธาตุมีอะตอมต่างกันตรงไหน
ครึ่งหลังจะพูดถึง แต่ละธาตุมีอะตอมต่างกันตรงไหน คำตอบตรงๆ เลยก็คือ จำนวนของอนุภาคย่อยจะไม่เท่ากัน ถึงตรงนี้เราจะรู้แล้วว่า โปรตอนกับนิวตรอน มันอยู่รวมกันตรงใจกลางที่เรียกว่านิวเคลียสของอะตอม ส่วนอิเล็กตรอนจะวิ่งวนรอบอะตอม ถ้ามีอิเล็กตรอนหลายตัว มันมีระบบการจัดเรียงวงโคจรอย่างไร แล้วการจัดเรียงอิเล็กตรอนนี้มันก็มาเกี่ยวกับตำแหน่งของธาตุในตารางธาตุด้วย
ความรู้ในเรื่อง อะตอม นี้จะนำมาใช้อธิบายหลายๆอย่างในเรื่องต่อไป
2. ตารางธาตุ
ตารางธาตุ จะแบ่งเนื้อหาเป็น 3 หัวข้อหลัก คือ “ก่อนจะมาเป็นตารางธาตุในปัจจุบัน” ต่อด้วย “พฤติกรรมของธาตุแต่ละกลุ่ม” และ “เจาะรายละเอียดธาตุกลุ่มสำคัญ”
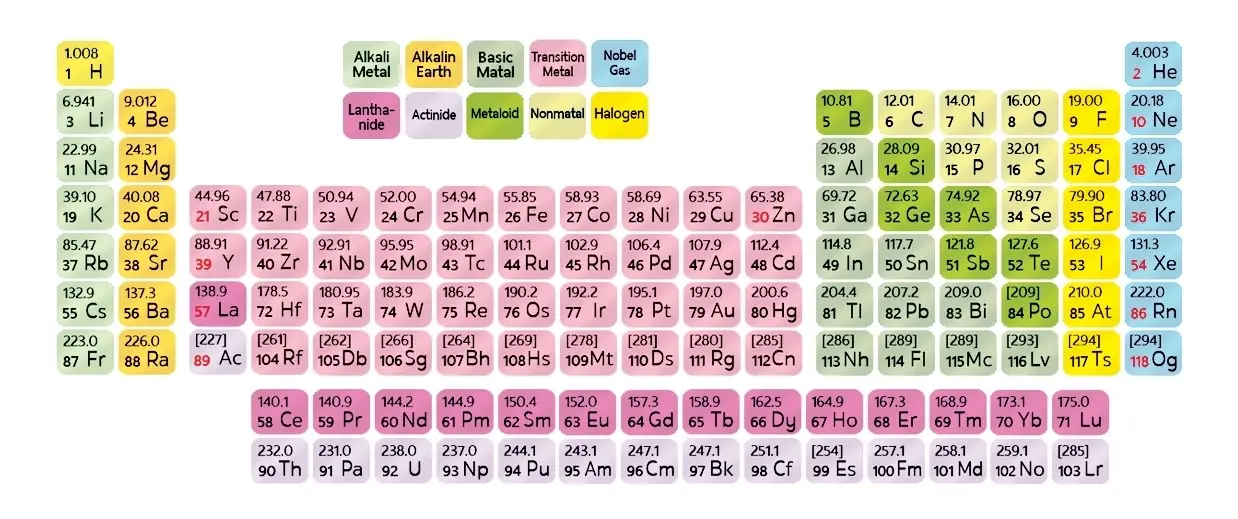
หัวข้อแรกคล้ายๆ เกริ่นนำเรื่องว่าเมื่อก่อนตารางธาตุไม่ได้มีหน้าตาแบบปัจจุบัน มีใครค้นพบอะไร ใช้หลักการแบบไหน จัดกลุ่มธาตุยังไง จนมาถึงการแบ่งธาตุเป็นกลุ่ม s กลุ่ม p กลุ่ม d กลุ่ม f
หัวข้อถัดมา พฤติกรรมของธาตุแต่ละกลุ่ม เมื่อนำธาตุแต่ละกลุ่มมาจัดหมู่ตามคุณสมบัติธาตุที่ใกล้เคียงกัน จะได้ธาตุหมู่ 1-18 โดยจุดสังเกตจะอยู่ที่หมู่แก๊สเฉื่อย (ธาตุหมู่ 18 หรือ 8A) ซึ่งเฉื่อยสมชื่อ ไม่ค่อยทำปฏิกิริยากับธาตุอื่นเพราะมันมีเสถียรภาพในตัวเองสูง อะไรที่ทำให้เกิดเสถียรภาพนี้ล่ะ และธาตุหมู่อื่นๆ ที่ยังไม่เสถียร ก็อยากจะมีเสถียรภาพ จะอธิบายผ่าน “กฎออกเตท” (Octet rule) ว่ามีได้ 2 พฤติกรรมคือ รับอิเล็กตรอนเพิ่มเข้ามา หรือไม่ก็ จ่ายอิเล็กตรอนของตัวเองออกไป จนมีการจัดเรียงอิเล็กตรอนที่เสถียรมากขึ้น ไฮไลต์จะอยู่ที่ “มีปัจจัยอะไรบ้างที่ส่งผลต่อพฤติกรรมรับ/จ่ายอิเล็กตรอนนี้ ก็จะมีการนำธาตุต่างๆ มาวัดค่าเปรียบเทียบกัน ไม่ว่าจะเป็น ขนาดอะตอม ค่า IE ค่า EN ความว่องไวต่อปฏิกิริยา ฯลฯ
หัวข้อสุดท้ายจะ เจาะรายละเอียดธาตุกลุ่มสำคัญ ซึ่งก็คือหมู่ 1A, 2A, 6A, 7A, ธาตุแทรนซิชัน และธาตุกัมมันตรังสี
3. พันธะเคมี
พันธะเคมี จะเกี่ยวกับพฤติกรรมรับ/จ่ายอิเล็กตรอนของธาตุ ธาตุจะรับจากอะตอมไหน หรือจ่ายให้อะตอมใด จะทำได้ก็ต้องมีธาตุมากกว่า 1 อะตอมมาเจอกัน มีปฏิสัมพันธ์กัน หรือเรียกว่าสร้างพันธะกัน
โดยเราจะแบ่งธาตุเป็น 2 กลุ่มใหญ่ๆ ก่อนคือ ธาตุโลหะ กับ ธาตุอโลหะ ด้วยเส้นขั้นบันไดในตารางธาตุ แล้วมาดูว่าธาตุที่จะสร้างพันธะกันนั้นเป็นธาตุกลุ่มไหน มี 3 กรณีหลักๆ คือ
- อโลหะ + อโลหะ มักจะสร้างพันธะโคเวเลนต์
- อโลหะ + โลหะ มักจะสร้างพันธะไอออนิก
- โลหะ + โลหะ ก็จะสร้างพันธะโลหะ
ซึ่งเราจะดูกันไปทีละกรณี
- พันธะโคเวเลนต์ (อโลหะ + อโลหะ) เมื่อหลายอะตอมมาอยู่รวมกันเป็น “โมเลกุล” พันธะที่ยึดอะตอมไว้ด้วยด้วย เกิดขึ้นยังไง มีกี่รูปแบบ มีรูปร่างโมเลกุลกี่แบบ สภาพขั้วพันธะเกิดขึ้นจากอะไร สร้างแรงดึงดูดระหว่างโมเลกุลได้ยังไง
- พันธะไอออนิก (อโลหะ + โลหะ) มีขั้นตอนการเกิดยังไง (วัฏจักรบอร์น-ฮาเบอร์ / Born-Habor) มีหลักการเรียกชื่อ มีสมบัติอะไรบ้าง เช่น การละลายน้ำ มีหลักการวิเคราะห์อย่างไรว่าสารนั้นจะละลายน้ำได้หรือไม่ ไปจนถึงการผสมสารละลายเข้าด้วยกันแล้วเกิดปฏิกิริยาตกตะกอน (สมการไอออนิก)
- พันธะโลหะ (โลหะ + โลหะ) มีรูปแบบการเกิดพันธะยังไง ซึ่งใช้อธิบายสมบัติของโลหะได้ เช่น ทำไมโลหะถึงเงาวับ ตีแผ่ขึ้นรูปได้ง่าย นำไฟฟ้า/นำความร้อนได้ดี
เนื้อหาทั้ง 3 เรื่องนี้ อะตอม ตารางธาตุ พันธะเคมี เป็นพื้นฐานสำคัญมาก เพราะใช้อธิบายเหตุผลต่างๆ ในเนื้อหาเคมี ม.5-6 เช่น บทเคมีอินทรีย์จะใช้ความรู้พันธะเคมีค่อนข้างเยอะ บทไฟฟ้าเคมีก็ใช้พื้นฐานเรื่องตารางธาตุ
ดูวิดีโอเพิ่มเติมเกี่ยวกับสรุปเคมี ม.4 เทอม 1 เข้าใจภาพรวมทั้งเทอมได้ ภายใน 6 นาที ได้ในคลิปนี้
น้องสามารถเข้าใจทั้ง 3 เรื่องนี้ (อะตอม ตารางธาตุ พันธะเคมี พร้อมได้ฝึกโจทย์มากกว่า 700 คำถาม) ใน คอร์สเรียนเคมี STEP UP เคมี ม.4 เทอม1 (ความยาวคลิป 18 ช.ม.) ได้ครบทั้งเนื้อหาและโจทย์โดยใช้เวลาเรียนประมาณ 24-30 ช.ม. เท่านั้น ก็จบทั้งเทอมนี้แล้ว กดสมัครได้เลยที่นี่

